
-
中文 | EN

中文 | EN
发布时间:2025-05-06 00:00:00.0
肌酸(creatine)作为人体能量代谢的核心分子,在肌肉和脑组织中发挥着"能量缓冲剂"的关键作用。特别是在神经元高强度工作时,它能快速补充ATP,确保大脑功能的正常运转。肌酸转运蛋白CRT(SLC6A8)负责将肌酸转运至细胞内,以满足组织的高能量需求。CRT的遗传突变会导致X连锁肌酸转运蛋白缺陷(CTD),其特征是大脑中肌酸缺乏,临床表现包括严重智力障碍、癫痫、自闭症、发育迟缓和运动功能障碍等。目前,该疾病尚缺乏有效的治疗手段。值得注意的是,处于II期临床试验的化合物RGX-202,正是通过竞争性抑制CRT的肌酸转运功能,有效诱导肿瘤细胞凋亡并抑制结直肠癌的生长。
2025年5月5日,中国科学院上海有机化学研究所生物与化学交叉研究中心于杰课题组在Cell Discovery杂志发表了题为"Transport and inhibition mechanisms of human creatine transporter"的研究论文。该研究首次报道了人源CRT蛋白在apo状态、底物creatine结合状态以及抑制剂RGX-202结合状态下的冷冻电镜结构。通过结合分子动力学模拟和功能实验,研究团队阐明了CRT识别底物和抑制剂的分子机制,并利用荧光显微镜技术深入探究了致病突变对CRT功能及细胞定位的影响。
基于解析的creatine和RGX-202结合结构,研究团队提出:creatine首先以向外开放的构象结合到中心位点,在Na+和Cl-的参与下发生构象变化,转变为向内封闭的状态暴露于细胞质侧,随后与Na+一起以内向开放的构象释放到细胞质中。值得注意的是,Cl-在整个过程中保持在其保守位置而不被释放。而抑制剂RGX-202则通过直接竞争creatine的结合位点来抑制CRT功能(图1)。
该研究首次在原子层面阐明了CRT的底物识别和抑制的分子机制,为未来开发针对CTD的治疗药物提供了重要的理论依据和结构基础。
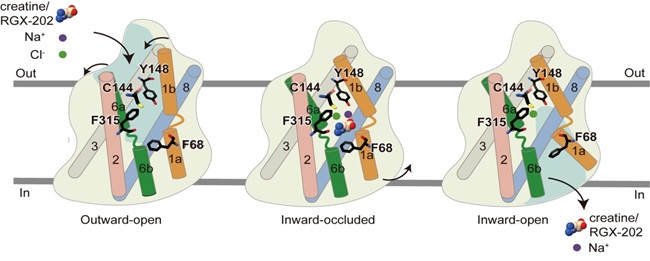
图1. CRT识别底物creatine和抑制剂RGX-202的分子机制。
中国科学院上海有机化学研究所生物与化学交叉研究中心博士研究生陈佳慧、张一敏,北京大学定量生物学中心陈楠浩博士为本文共同第一作者。于杰研究员为本文通讯作者。该工作得到了上海市基础研究、上海市老龄化研究重点实验室和上海浦江计划的资助。
论文链接:https://www.nature.com/articles/s41421-025-00801-4
